ฟิสิกส์นิวเคลียร์
ฟิสิกส์นิวเคลียร์
ปฎิกิริยานิวเคลียร์ คือ กระบวนการที่นิวเคลียสเปลี่ยนแปลงองค์ประกอบหรือระดับพลังงาน ในทุกสมการปฏิกิริยานิวเคลียร์ ผลบวกของเลขอะตอมทั้งก่อนและหลังปฏิกิริยาจะต้องเท่ากัน ซึ่ง แสดงว่าประจุไฟฟ้ารวมมีค่าคงตัว และผลบวกของเลขมวลก่อนและหลังปฏิกิริยาก็จะต้องเท่ากัน ด้วย ซึ่งแสดงว่า จำนวนนิวคลียสรวมก่อนและหลังปฏิกิริยาจะต้องคงตัว
การพบกัมมันตภาพรังสี
ในปี ค.ศ. 1896 เบ็กเคอเรล ( Henri Becquerel ) ได้ทำการทดลองการเรืองแสงของสารต่าง ๆ และได้พบว่าสารประกอบของยูเรเนียมสามารถ แผ่รังสีชนิดหนึ่งออกมาได้เองตลอดเวลาโดยไม่ ขึ้นอยู่กับ สภาพแวดล้อมเลย และจากการศึกษาเบื้องต้นของเบ็กเคอเรล เขาได้พบว่า รังสีนี้มีสมบัติ บางประการ คล้ายรังสีเอกซ์ เช่น สามารถทะลุผ่านวัตถุบางชนิดและทำให้อากาศแตกตัวเป็นไอออน ได้
ต่อมา ปีแอร์ คูรี ( Pierre Curie ) และมารี คูรี ( Maric Curie ) ได้ทำการทดลองกับธาตุอื่น ๆ อีกหลายชนิด และพบว่าธาตุบางชนิดมีการแผ่รังสีเช่นเดียวกับธาตุยูเรเนียม ปรากฏการณ์ที่ธาตุ แผ่รังสีได้เองอย่างต่อเนื่องนี้ เรียกว่า กัมมันตภาพรังสี ( radioactivity ) และธาตุที่มีการแผ่รังสีได้ เองเรียกว่า ธาตุกัมมันตรังสี (radioactive element) จากการศึกษารังสีที่แผ่ออกมาจากธาตุ กัมมันตรังสีทั่วไป
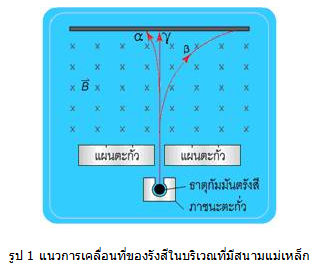

เราทราบแล้วว่า อนุภาคที่มีประจุไฟฟ้าเมื่อเคลื่อนที่ในบริเวณที่มีสนามแม่เหล็กจะเกิดแรง กระทำ ต่ออนุภาคทำให้ทิศการเคลื่อนที่เปลี่ยนไป ทำให้ทราบว่ารังสีแอลฟามีประจุไฟฟ้าบวก รังสี บีตามีประจุไฟฟ้าลบและรังสีแกมมามีสภาพเป็นกลางทางไฟฟ้า
การศึกษารังสีทั้งสามชนิด ทำให้ทราบสมบัติต่าง ๆ ของรังสีเหล่านี้เพิ่มขึ้นดังนี้
รังสีแอลฟา มีส่วนประกอบเป็นนิวเคลียสของธาตุฮีเลียมมีมวลประมาณ 4u มีประจุไฟฟ้า +2e มีพลังงานประมาณ 4-10 MeV รังสีแอลฟาสามารถทำให้สารที่รังสีผ่านแตกตัวเป็นไอออนได้ดีจึงเสีย พลังงานอย่างรวดเร็ว รังสีแอลฟาจึงมีอำนาจทะลุผ่านน้อยมากกล่าวคือสามารถวิ่งผ่านอากาศได้ ประมาณ 3-5 เซนติเมตร และเมื่อใช้แผ่นกระดาษบาง ๆ กั้น รังสีแอลฟาก็ทะลุผ่านไม่ได้ เนื่องจาก รังสีนี้คือนิวเคลียสที่เป็นอนุภาค บางครั้งจึงเรียกรังสีแอลฟาว่า อนุภาคแอลฟา
รังสีบีตา เป็นอนุภาคที่มีประจุไฟฟ้า -1e มีมวลเท่ากับมวลของอิเล็กตรอน รังสีบีตา คือ อิเล็กตรอน ( ที่มาจากการสลายของนิวเคลียส มิใช่อิเล็กตรอนที่เคลื่อนที่รอบนิวเคลียส ) มีพลังงาน ตั้งแต่ 0.04-3.2 MeV รังสีบีตาสามารถวิ่งผ่านไปในอากาศได้ประมาณ 1-3 เมตร อำนาจทะลุผ่าน ของรังสีบีตาจึงมากกว่ารังสีแอลฟา บางครั้งเรียกรังสีบีตาว่า อนุภาคบีตา
รังสีแกมมา เป็นรังสีที่มีสภาพเป็นกลางทางไฟฟ้ามีสมบัติของคลื่นแม่เหล็กไฟฟ้า รังสีแกมมา มีพลังงานประมาณ ตั้งแต่ 0.04-3.2 MeV สามารถทะลุผ่านแผ่นอะลูมิเนียม ที่หนาหลายเซนติเมตร ได้ จึงมีอำนาจทะลุผ่านมากที่สุดในบรรดารังสีทั้งสามชนิด
การเปลี่ยนสภาพนิวเคลียส
ในการศึกษาธาตุกัมมันตรังสีต่าง ๆ พบว่า มีธาตุใหม่เกิดขึ้นหลังจากที่ได้แผ่รังสีแอลฟา หรือรังสีบีตาเสมอ เช่น เมื่อทอเรียมปล่อยอนุภาคแอลฟาออกมาจะกลายเป็นเรเดียม ซึ่งมีมวลอะตอม น้อยกว่าทอเรียมประมาณเท่ากับมวลของอนุภาคแอลฟาที่ปลดปล่อยออกมา นอกจากนี้ประจุไฟฟ้า ของนิวเคลียสของเรเดียมที่เกิดใหม่ก็มีค่าน้อยกว่าของทอเรียมเดิมอยู่ +2e ด้วย เนื่องจากมวลของ ธาตุ 1 อะตอมมีค่าใกล้เคียงกับมวลของนิวเคลียสดังที่ทราบมาแล้ว ดังนั้นการเปลี่ยนแปลงของ นิวเคลียส ทั้งนี้เนื่องจากมวลของอิเล็กตรอนมีค่าน้อยมาก เมื่อเปรียบเทียบกับมวลของโปรตอน แสดงว่าอนุภาคแอลฟาได้มาจากการเปลี่ยนสภาพนิวเคลียส (nuclear transformation) ของ ทอเรียมไปเป็นเรเดียม
ในกรณีที่มีการแผ่รังสีบีตา เช่น เมื่อตะกั่วปล่อยอนุภาคบีตาออกมา ตะกั่ว จะกลายเป็นบิสมัท ซึ่งมีประจุเพิ่มขึ้น +1e แต่ทั้งตะกั่วและบิสมัทจะมีมวลใกล้เคียงกัน พลังงานจลน์ของอิเล็กตรอนหรือ อนุภาคบีตาที่ออกมานี้มีค่าสูงมากเมื่อเทียบกับพลังงานจลน์ของอิเล็กตรอนที่เคลื่อนที่รอบนิวเคลียส แสดงว่าอนุภาคบีตานี้ไม่ใช่อิเล็กตรอนที่เคลื่อนที่รอบนิวเคลียส นั่นคืออนุภาคบีตานี้ต้องเกิดจากการ เปลี่ยนสภาพนิวเคลียส
ด้วยเหตุที่กัมมันตภาพรังสีมีความเกี่ยวข้องกับการเปลี่ยนสภาพของนิวเคลียสการศึกษาเกี่ยวกับ กัมมันตภาพรังสีจะทำให้ทราบองค์ประกอบของนิวเคลียสได้
องค์ประกอบของนิวเคลียส
รัทเทอร์ฟอร์ดให้การสนับสนุนแนวคิดที่ว่านิวเคลียสของไฮโดรเจนเป็นองค์ประกอบของ นิวเคลียส ของธาตุต่างๆ โดยทดลองยิงอนุภาคแอลฟาชนนิวเคลียสของไนโตรเจน และพบว่ามี นิวเคลียสของ ออกซิเจนและไฮโดรเจนเกิดขึ้น ดังรูป 2 เขาจึงเสนอให้เรียกนิวเคลียสของไฮโดรเจน ว่า โปรตอน และจากการที่ธาตุกัมมันตรังสีบางธาตุมีการปล่อยอนุภาคบีตาหรืออิเล็กตรอนออกมา ทำ ให้นักวิทยาศาสตร์ บางคนคิดว่า อิเล็กตรอนก็อาจเป็นองค์ประกอบของนิวเคลียสของธาตุต่าง ๆ ได้ เช่นกัน ด้วยเหตุนี้จึงได้มี การสร้างสมมติฐานโปรตอน – อิเล็กตรอน
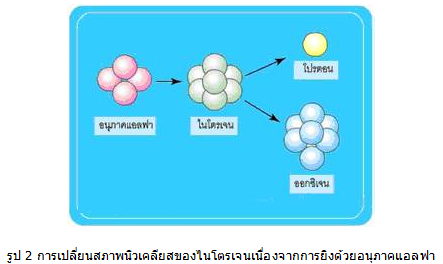
สมมติฐาน โปรตอน – อิเล็กตรอน กล่าวว่า นิวเคลียสประกอบด้วยโปรตอนและอิเล็กตรอน ซึ่ง สามารถอธิบายการแผ่รังสีแอลฟาได้ กล่าวคือ อนุภาคแอลฟาเกิดจากการรวมตัวกันระหว่างโปรตอน 4 ตัว และอิเล็กตรอน 2 ตัว แล้วหลุดออกมาจากนิวเคลียส ส่วนการแผ่รังสีบีตานั้นเกิดจากการปล่อย อิเล็กตรอน ในนิวเคลียสออกมา แต่จากหลักความไม่แน่นอนของไฮเซนเบอร์กข้อมูลนี้ชี้ให้เห็นว่า อิเล็กตรอนจะอยู่ใน นิวเคลียสไม่ได้ เนื่องจากมีพลังงานสูงมาก สมมติฐานจึงต้องยกเลิกไป
การพบนิวตรอน
การทดลองยิงอนุภาคแอลฟาพุ่งชนนิวเคลียสของธาตุเบริลเลียมได้รังสีออกมาชนิดหนึ่งมี สภาพเป็น กลางทางไฟฟ้า แชดวิก (Sir James Chadwick 1819 - 1974) นักฟิสิกส์ ชาวอังกฤษ นำผลการทดลอง นี้มาวิเคราะห์ แล้วเสนอว่ารังสีที่ได้คือ อนุภาคนิวตรอน ซึ่งเป็นการสนับสนุน แนวคิดของรัทเทอร์ฟอร์ดที่ว่า นิวเคลียส มีอนุภาคนิวตรอน
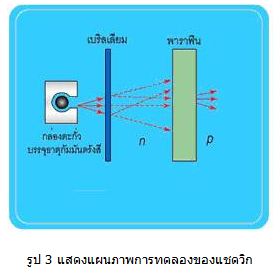
เมื่อแชดวิกพบอนุภาคนิวตรอนแล้ว ได้มีการตั้งสมมติฐานเรื่องโครงสร้างของนิวเคลียสใหม่ เรียก สมมติฐานโปรตอน – นิวตรอน ด้วยแนวคิดที่ว่า นิวเคลียสประกอบด้วยอนุภาคโปรตอนและอนุภาค นิวตรอนรวมกันเรียกว่า นิวคลีออน ส่วนจำนวนโปรตอนและจำนวนนิวตรอนรวมกัน เรียกว่า เลขมวล จำนวนโปรตอนอย่างเดียวในนิวเคลียส เรียกว่าเลขอะตอม


การสลายตัวให้รังสีเบตา (β - decay)
นิวเคลียสที่มีจำนวนนิวตรอนมากเกินไป เมื่อเทียบกับจำนวนโปรตอนทำให้นิวเคลียสไม่เสถียร จึงเกิดการสลายให้รังสีเบตา โดยนิวเคลียสใหม่จะมีเลขมวลเท่าเดิม แต่เลขอะตอมจะมากกว่า ของนิวเคลียสตั้งต้นอยู่ 1 หน่วย ดังนี้
ตัวอย่างเช่น


การสลายของนิวเคลียสกัมมันตรังสี
ธาตุกัมมันตรังสีชนิดหนึ่งสลายตัวเกิดธาตุใหม่ หากธาตุใหม่เป็นธาตุกัมมันตรังสี (นิวเคลียสไม่เสถียร) ก็จะสลายตัวต่อไปอีกเรื่อย ๆ จนกว่าจะเกิดธาตุใหม่ที่มีนิวเคลียสที่เสถียร
อนุกรมการสลายตัวในธรรมชาติที่น่าสนใจ ได้แก่
1. อนุกรมของยูเรเนียม-238 เริ่มต้นที่ U-238 สุดท้ายที่ Pb-206
2. อนุกรมของยูเรเนียม-235 เริ่มต้นที่ U-235 สุดท้ายที่ Pb-207
3. อนุกรมทอเรียม232 เริ่มต้นที่ Th-232 สุดท้ายที่ Pb-208
สมมติฐานรัทเทอร์ฟอร์ดและซอดดี
1. ธาตุกัมมันตรังสีสลายให้ธาตุใหม่โดยปล่อยอนุภาคแอลฟา อนุภาคเบตา ธาตุใหม่ที่ได้จะมีสมบัติทางเคมีต่างไปจากธาตุเดิม และธาตุใหม่อาจเป็นธาตุกัมมันตรังสีก็ ได้
2. การสลายตัวของธาตุกัมมันตรังสี ไม่ขึ้นกับสภาพแวดล้อมภายนอกนิวเคลียส เป็นต้นว่า อุณหภูมิ ความดัน ทุกนิวเคลียสมีโอกาสสลายได้เท่า ๆ กัน แต่บอกไม่ได้ว่านิวเคลียสใดสลายก่อนหรือหลัง


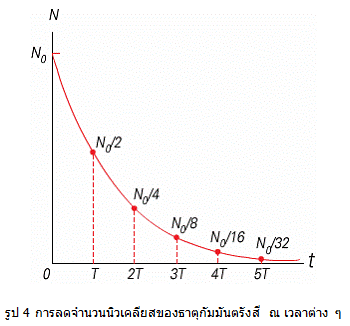
จากกราฟแสดงจะเห็นครึ่งชีวิตของธาตุกัมมันตรังสี



ไอโซโทป

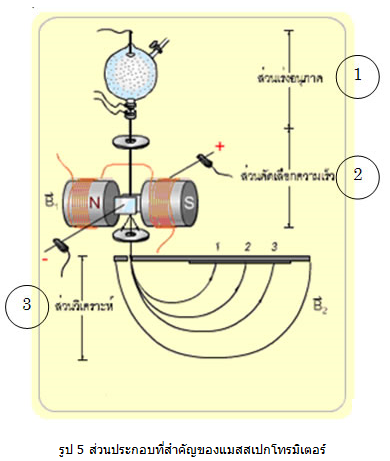
แมสสเปกโทรมิเตอร์ (Mass Spectrometer)
เป็นเครื่องมือวิเคราะห์มวลอะตอมของธาตุต่าง ๆ รวมทั้งการวิเคราะห์ไอโซโทปของธาตุชนิดเดียวกันด้วย โดยอาศัยหลัก
1. สมบัติทางกายภาพของไอโซโทปต่างกัน
2. อนุภาคมีประจุไฟฟ้า เคลื่อนที่ในสนามไฟฟ้าและสนามแม่เหล็ก

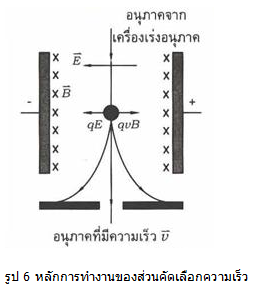
อนุภาคที่คัดความเร็วได้พอเหมาะจะทำให้แรงทั้งสองมีค่าเท่ากันเป็นผลให้อนุภาคเคลื่อนที่ผ่าน
สนามทั้งสองในแนวเดิม

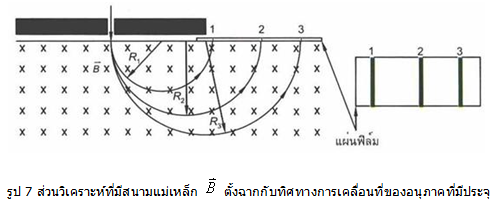
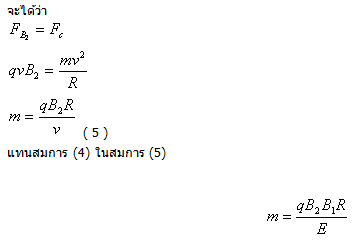
จากสมการ (5) แสดงว่า มวลของอนุภาคแปรผันตรงกับรัศมีความโค้ง และเนื่องจาก มวลของแต่ละไอโซโทปแตกต่างกัน ดังนั้นรัศมีความโค้งของแต่ละไอโซโทปจะแตกต่างกัน
เสถียรภาพนิวเคลียส
1 แรงนิวเคลียร์
นิวเคลียสมีลักษณะเป็นทรงกลม ขนาดของนิวเคลียสขึ้นอยู่กับจำนวนนิวคลีออนในนิวเคลียส นิวคลีออน คือ จำนวนโปรตอนและจำนวนนิวตรอนในนิวเคลียสนั่นเอง

แรงนิวเคลียร์ เป็นแรงที่ยึดนิวคลีออนไว้ด้วยกันที่ นิวเคลียสแรงนี้มีค่ามากพอที่จะต้านแรง ผลักระหว่างประจุไฟฟ้า ของนิวคลีออน ซึ่งมีค่าสูงมาก เนื่อง จากนิวเคลียสมีขนาดเล็กมากนั่นเอง ขณะเดียวกันความหนาแน่นของนิวเคลียส มีค่าประมาณ 1018 กิโลกรัมต่อลูกบาศก์เมตร ในขณะที่ ความหนาแน่น ของธาตุที่มีความหนาแน่นมากที่สุด (ธาตุออสเมียม) มีค่าเท่ากับ 2 × 1014 กิโลกรัม ต่อลูกบาศก์เมตร เปรียบเทียบกันจะเห็นว่า นิวคลีออน ในนิวเคลียสอยู่อย่างหนาแน่นมาก แรงนิวเคลียร์จึงเป็นแรงที่มีค่าสูงมาก
2 พลังงานยึดเหนี่ยว
พลังงานยึดเหนี่ยว คือ พลังงานที่ยึดนิวคลีออนไว้ด้วยกัน ในนิวเคลียสการที่จะกระทำ ให้นิวคลีออนแยกตัวออกจาก



