ปฏิกิริยาเคมี
บทเรียนที่ 1 ปฏิกิริยาเคมี
ปฏิกิริยาเคมี คือ กระบวนการเปลี่ยนของสารตั้งต้นไปเป็นสารใหม่ โดยปริมาณสารตั้งต้นจะลดลง และปริมาณสารใหม่จะเกิดขึ้น และเพิ่มปริมาณขึ้นเรื่อยๆ เมื่อเวลาผ่านไป โดยสามารถเขียนให้เข้าใจง่ายด้วยสมการเคมี
ปฏิกิริยาเคมีจำแนกเป็น 2 ประเภท คือ
1. ปฏิกิริยาเคมีสมบูรณ์ คือ การเกิดสารใหม่ขณะที่สารตั้งต้นตัวใดตัวหนึ่งหมดไปหรือหมดทุกตัว
2. ปฏิกิริยาเคมีไม่สมบูรณ์ คือ การเกิดสารใหม่ขณะที่สารตั้งต้นยังเหลือทุกตัว ไม่มีตัวใดตัวหนึ่งหมดไป
ทฤษฎีที่เกี่ยวข้องกับปฏิกิริยาเคมี
1. ทฤษฎีการชนโมเลกุล (Collision Theory) กล่าวถึง โมเลกุลของสารต้องมีการชนซึ่งกันและกัน ซึ่งการชนกันแต่ละครั้งไม่จำเป็นต้องเกิดปฏิกิริยา
2. ทฤษฎีจลน์ของโมเลกุล (Kinetic Theory) กล่าวถึง โมเลกุลต้องมีการเคลื่อนที่ช้าลง ซึ่งก่อให้เกิดพลังงานจลน์ โดยโมเลกุลต้องมีพลังงานสูงพอจึงจะเกิดปฏิกิริยาได้
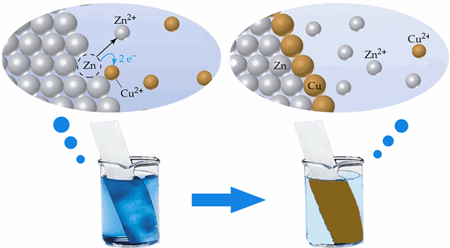
สถานะการเกิดปฏิกิริยาเคมี
1. ต้องมีจำนวนโมเลกุลมากพอ
2. ต้องมีการชนกันระหว่างโมเลกุล
3. ต้องมีพลังงานสูงพอ โดยอย่างน้อยต้องเท่ากับพลังงานก่อกัมมันต์
4. ต้องมีทิศทางที่เหมาะสม
ศาสตร์ทางเคมีที่เกี่ยวข้องกับการศึกษาอัตราการเกิดปฏิกิริยาเคมี เรียกว่า จลนศาสตร์เคมี (chemical kinetics) โดยคำว่า จลนศาสตร์ มีความหมายเกี่ยวข้องกับการเคลื่อนที่ของสาร ซึ่งเกี่ยวข้องกับอัตราการเกิดปฏิกิริยาเคมี (Rate of chemical reaction) โดยการเกิดปฏิกิริยาหนึ่งๆที่อยู่ในสภาวะเดียวกันจะมีอัตราการเกิดปฏิกิริยาเฉพาะค่า โดยขึ้นอยู่กับสภาวะธรรมชาติของสารนั้นๆ เช่น อัตราการเกิดปฏิกิริยาของก๊าซไฮโดรเจนกับก๊าซฟลูออรีน และก๊าซไนโตรเจน
H2 (g) + F2 (g) = 2HF อัตราการเกิดปฏิกิริยาเร็ว
3H2 (g) + N2 (g) = 2NH3 อัตราการเกิดปฏิกิริยาช้า
Return to contents
อัตราการเกิดปฏิกิริยาเคมี
อัตราการเกิดปฏิกิริยาเคมี (Rate of chemical reaction) หมายถึง การเปลี่ยนแปลงปริมาณสารในหนึ่งหน่วยเวลาของการเกิดปฏิกิริยาของสารนั้น
อัตราการเกิดปฏิกิริยาเคมี = ปริมาณสารตั้งต้นที่ลดลง
**********************************เวลา
อัตราการเกิดปฏิกิริยาเคมี = ปริมาณสารที่เปลี่ยนไป
*********************************เวลา
อัตราการเกิดปฏิกิริยาเคมี = ปริมาณสารที่เพิ่มขึ้น
********************************เวลา
ชนิดอัตราการเกิดปฏิกิริยาเคมี แบ่งเป็น 2 ชนิด
1. อัตราการเกิดปฏิกิริยาเฉลี่ย หมายถึง อัตราการเกิดปฏิกิริยาที่คำนวณจากการเปลี่ยนแปลงปริมาณสารทั้งหมดในหนึ่งหน่วยเวลา
2. อัตราการเกิดปฏิกิริยา ณ ขณะใดขณะหนึ่ง หมายถึง อัตราการเกิดปฏิกิริยาที่คำนวณจากการเปลี่ยนแปลงปริมาณสารในช่วงเวลาใดเวลาหนึ่ง
สรุปประเด็นที่เกี่ยวข้อง
1. ปฏิกิริยาเคมีหนึ่งๆ จะมีขั้นตอนการเกิดปฏิกิริยาหลายขั้นตอน ทั้งขั้นที่เกิดเร็ว และขั้นที่เกิดช้า โดยมีขั้นสำหรับควบคุมปฏิกิริยาหรือขั้นกำหนดอัตรา (Rate determing step) คือ ขั้นที่ดำเนินไปที่ช้าที่สุด
2. ขณะที่การเกิดปฏิกิริยาเคมีดำเนินไป ปฏิกิริยาเคมีในขั้นเริ่มต้นจะมีอัตราการเกิดที่รวดเร็ว เนื่องจากปริมาณสารตั้งต้นมีมาก และเมื่อปฏิกิริยาผ่านไประยะหนึ่ง อัตราการเกิดปฏิกิริยาจะช้าลงเมื่อเทียบกับในช่วงเริ่มต้น เนื่องจากปริมาณสารตั้งต้นมีปริมาณลดลง
3. สารเคมีแต่ละชนิดในปฏิกิริยาเคมีจะมีอัตราเร็วไม่เท่ากัน
4. การคำนวณหาอัตราการเกิดปฏิกิริยา สามารถหาได้จากสารใดก็ได้ ด้วยวิธี คือ
– หากเป็นของแข็ง สามารถหาได้โดยการชั่งน้ำหนัก
– หากเป็นของเหลว สามารถหาได้โดยการชั่งน้ำหนักหรือการวัดปริมาณ
– หากเป็นสารละลาย สามารถหาได้จากความเข้มข้น
– หากเป็นก๊าซ สามารถหาได้โดยการวัดปริมาตรหรือวัดความดัน
5. การหาอัตราการเกิดปฏิกิริยาเคมี สามารถหาได้จากสารตัวใดตัวหนึ่งก็ได้ ซึ่งจะให้ค่าที่เท่ากัน ตามสูตรด้านล่าง
อัตราการเปลี่ยนแปลงของสาร = ΔA ↔ ΔB ↔ ΔC ↔ ΔD
–Δt –Δt +Δt +Δt
อัตราการเกิดปฏิกิริยาเคมี = ΔA ↔ ΔB ↔ ΔC ↔ ΔD
-Δt -3Δt +2Δt +4Δt
หมายเหตุ: Δ = ผลต่าง, t = เวลา, + = การเพิ่มขึ้น, – = การลดลง
Return to contents
ม.5
ม.6
นักเรียน
-
7203 ปฏิกิริยาเคมี /lesson-chemistry/item/7203-2017-06-09-13-16-10เพิ่มในรายการโปรด
สถาบันส่งเสริมการสอนวิทยาศาสตร์และเทคโนโลยี (สสวท.) กระทรวงศึกษาธิการ เป็นหน่วยงานของรัฐที่ไม่แสวงหากำไร ได้จัดทำเว็บไซต์คลังความรู้ SciMath เพื่อส่งเสริมการสอนวิทยาศาสตร์ คณิตศาสตร์และเทคโนโลยีทุกระดับการศึกษา โดยเน้นการศึกษาขั้นพื้นฐานเป็นหลัก หากท่านพบว่ามีข้อมูลหรือเนื้อหาใด ๆ ที่ละเมิดทรัพย์สินทางปัญญาปรากฏอยู่ในเว็บไซต์ โปรดแจ้งให้ทราบเพื่อดำเนินการแก้ปัญหาดังกล่าวโดยเร็วที่สุด
The Institute for the Promotion of Teaching Science and Technology (IPST), Ministry of Education, a non-profit organization under the Thai government, developed SciMath as a website that provides educational resources in Science, Mathematics and Technology. IPST invites visitors to use its online resources for personal, educational and other non-commercial purpose. If there are any problems, please contact us immediately.
Copyright © 2018 SCIMATH :: คลังความรู้ SciMath. Terms and Conditions. Privacy. , All Rights Reserved.
อีเมล: This email address is being protected from spambots. You need JavaScript enabled to view it. (ให้บริการในวันและเวลาราชการเท่านั้น)