สารละลาย (solution)
การละลายของสารในตัวทำละลาย
สารชนิดเดียวกันละลายในตัวทำละลายต่างชนิดได้แตกต่างกัน คือ
1) สารบางชนิดอาจไม่ละลายน้ำ แต่ละลายในตัวทำละลายชนิดอื่น เช่น ลูกเหม็น เชลแล็ก ไม่ละลายน้ำ แต่ละลายในแอลกอฮอล์
2) สารบางชนิดอาจละลายได้ในตัวทำละลายหลายชนิด เช่น สีผสมอาหารละลายในน้ำ และละลายในแอลกอฮอล์
เมื่อใช้น้ำเป็นตัวทำละลาย สามารถแบ่งสารออกเป็น 2 ประเภท คือ สารที่ละลายน้ำ และสารที่ไม่ละลายน้ำ จะเห็นว่าสารต่างชนิดกันละลายน้ำได้ต่างกัน
ถ้าตัวละลายเป็นของแข็งละลายในตัวทำละลายที่เป็นของเหลว ตัวละลายจะแพร่ในตัวทำละลาย เมื่อตัวละลายละลายหมด จะมองเห็นสารละลายเป็นเนื้อเดียวกัน ไม่มีตะกอน เนื่องจากตัวละลายที่เป็นของแข็งแทรกอยู่ในตัวทำละลาย เช่น การละลายของน้ำตาลในน้ำ การละลายของเกลือในน้ำ เป็นต้น ในกรณีที่ตัวละลายไม่ละลายในตัวทำละลาย แสดงว่าตัวละลายไม่สามารถแทรกตัวในตัวทำละลายชนิดนั้นได้ จึงมองเห็นไม่เป็นเนื้อเดียวกัน
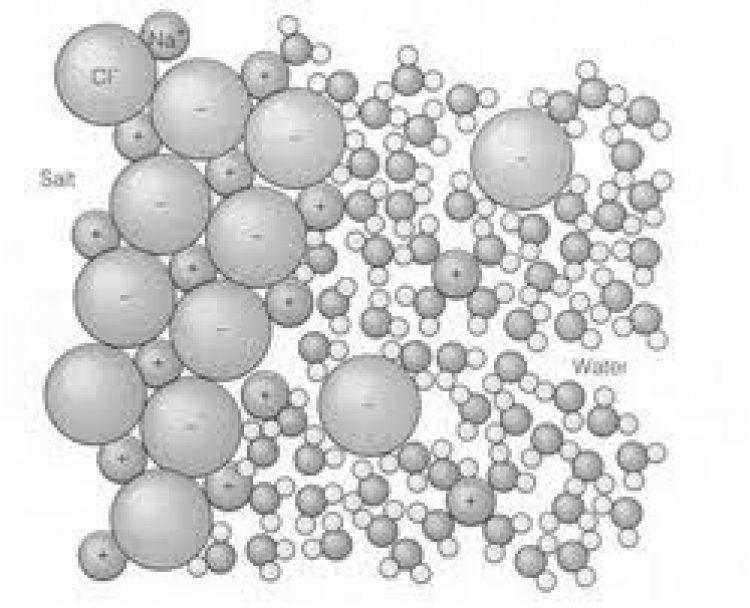
ภาพจำลองแสดงการละลายของเกลือ
ที่มา : Garrison (2007)
ความรู้เกี่ยวกับการละลายของสารในตัวทำละลายต่าง ๆ นำไปใช้ประโยชน์ในชีวิตประจำวันได้หลายประการ เช่น สามารถใช้ตัวทำละลายสลายคราบต่าง ๆ ที่ติดอยู่บนเสื้อผ้าได้ เช่น ใช้แอลกอฮอล์ (เอทานอล) ลบรอยหญ้าหรือรอยหมึกจาง ๆ , น้ำเกลือลบรอยเลือด , น้ำนมลบรอยหมึก หรือ การนำเชลแล็กไปละลายในแอลกอฮอล์ก่อนแล้วจึงนำสารละลายเชลแล็กไปทาไม้หรือเฟอร์นิเจอร์ เพื่อให้เกิดความสวยงามและรักษาเนื้อไม้ เป็นต้น
ประเภทของสารละลาย
สารละลายมีหลายประเภท หากใช้เกณฑ์ในการจำแนก จะแบ่งสารละลายออกเป็น 3 กลุ่ม ดังนี้
1. จำแนกตามสถานะของสารละลาย แบ่งเป็น 3 ประเภท คือ
1.1 ของแข็ง เช่น เหรียญบาท ทองเหลือง นาก
1.2 ของเหลว เช่น สารละลายคอปเปอร์ (II) ซัลเฟต น้ำเชื่อม น้ำเกลือ
1.3 แก๊ส เช่น แก๊สหุงต้ม อากาศ
2. จำแนกตามปริมาณของตัวละลาย แบ่งเป็น 2 ประเภท คือ
2.1 สารละลายอิ่มตัว (Saturated solution) คือ สารละลายที่ตัวละลายไม่สามารถละลายในตัวทำละลายได้เพิ่มขึ้นอีกเมื่อตัวทำละลายและอุณหภูมิคงที่ ซึ่งอาจเป็นสารละลายอิ่มตัวพอดี หรือสารละลายอิ่มตัวเหลือเฟือ ถ้าเพิ่มความร้อนให้สารละลายอิ่มตัวเหลือเฟือละลายได้อีก จะได้สารละลายอิ่มตัวยิ่งยวด
2.2 สารละลายไม่อิ่มตัว (Unsaturated solution) คือ สารละลายที่ตัวละลายยังสามารถละลายในตัวทำละลายได้อีก
3. จำแนกตามความเข้มข้น แบ่งเป็น 2 ประเภท คือ
3.1 สารละลายเข้มข้น คือ สารละลายที่ประกอบด้วยตัวละลายปริมาณมาก มีตัวทำละลายปริมาณน้อย
3.2 สารละลายเจือจาง คือ สารละลายที่ประกอบด้วยตัวละลายปริมาณน้อย มีตัวทำละลายปริมาณมาก
ความเข้มข้นของสารละลาย เป็นค่าที่แสดงให้ทราบถึงปริมาณของตัวละลายที่มีอยู่ในปริมาณของสารละลาย การบอกความเข้มข้นของสารละลายในหน่วยร้อยละ หรือเปอร์เซ็นต์ มี 3 หน่วย คือ
1. ร้อยละโดยมวลต่อมวล หรือร้อยละโดยมวล หรือเปอร์เซ็นต์โดยมวล (มวลต่อมวล) เป็นการบอกมวลของตัวละลายในสารละลาย 100 กรัม เช่น สารละลายเกลือแกงเข้มข้นร้อยละ 10 โดยมวล หมายความว่า มีเกลือแกงละลายอยู่ 10 กรัม ในสารละลาย 100 กรัม แสดงว่ามีน้ำเป็นตัวทำละลายเท่ากับ 90 กรัม เป็นต้น นิยมใช้กับสารละลายที่ทั้งตัวละลายและตัวทำละลายเป็นของแข็ง
การหาความเข้มข้นเป็นร้อยละโดยมวล หาได้จากสูตร
ร้อยละโดยมวล = มวลของตัวละลาย X 100
มวลของสารละลาย
2. ร้อยละโดยปริมาตรต่อปริมาตร หรือร้อยละโดยปริมาตร หรือเปอร์เซ็นต์โดยปริมาตร (ปริมาตรต่อปริมาตร) เป็นการบอกปริมาตรของตัวละลายที่ละลายในสารละลาย 100 หน่วยปริมาตร เช่น สารละลายแอลกอฮอล์เข้มข้นร้อยละ 25 โดยปริมาตร หมายความว่า มีแอลกอฮอล์ 25 ลูกบาศก์เซนติเมตร ละลายอยู่ในสารละลาย 100 ลูกบาศก์เซนติเมตร กรัม แสดงว่ามีน้ำเป็นตัวทำละลายเท่ากับ 75 ลูกบาศก์เซนติเมตร เป็นต้น นิยมใช้กับสารละลายที่ทั้งตัวละลายและตัวทำละลายเป็นของเหลว
กระบวนการเกิดสารละลาย เกิดจากสารชนิดหนึ่ง กระจายอยู่ในสาร อีกชนิดหนึ่ง ถ้ากระจายอย่างสม่ำเสมอ และมองเห็นเหมือนกันทุกส่วน มีลักษณะเป็นเนื้อเดียวกัน เรียกสารผสมนี้ว่า สารละลาย แต่ถ้ากระจายอยู่อย่างไม่สม่ำเสมอ โดยยังมองเห็นเป็นสารเดิมอยู่ เรียกสารผสมนี้ว่า สารเนื้อผสม สารเนื้อผสมที่มีอนุภาคเล็ก ๆ ของของแข็งกระจายอยู่ในของเหลว หรือแก๊ส เรียกว่า สารแขวนลอย
ในกระบวนการละลาย จะมีสารตัวหนึ่งเป็น ตัวทำละลาย และสารอีกตัวหนึ่งเป็น ตัวละลาย สารใดเป็นตัวทำละลาย หรือเป็นตัวละลาย พิจารณาได้ง่าย ๆ ดังนี้
1. ถ้าตัวละลาย และตัวทำละลายมีสถานนะต่างกัน สารที่มีสถานะเดียวกันกับสารละลาย จัดเป็นตัวทำละลาย สารที่มีสถานะต่างไปจากสารละลาย เป็นตัวละลาย
2. ถ้าตัวละลาย และตัวทำละลายมีสถานะเดียวกัน สารที่มีปริมาณน้อยกว่าจัดเป็นตัวละลาย สารที่มีปริมาณมากกว่า จัดเป็นตัวทำละลาย
ร้อยละโดยปริมาตร = ปริมาตรของตัวละลาย X 100
ปริมาตรของสารละลาย
3. ร้อยละโดยมวลต่อปริมาตร หรือเปอร์เซ็นต์โดยมวลต่อปริมาตร (มวลต่อปริมาตร) เป็นการบอกมวลของตัวละลายในสารละลาย 100 หน่วยปริมาตร ซึ่งโดยทั่วไปมวลตัวละลายมีหน่วยเป็นกรัม และปริมาตรของสารละลายมีหน่วยเป็นลูกบาศก์เซนติเมตร เช่น น้ำเชื่อมเข้มข้นร้อยละ 15 โดยมวลต่อปริมาตร หมายความว่า มีน้ำตาลทราย 15 กรัม ละลายในสารละลายปริมาตร 100 ลูกบาศก์เซนติเมตร เป็นต้น นิยมใช้กับสารละลายที่เป็นของเหลวโดยมีของแข็งเป็นตัวละลาย
การหาความเข้มข้นเป็นร้อยละโดยมวลต่อปริมาตร หาได้จากสูตร
ร้อยละโดยมวลต่อปริมาตร = มวลของตัวละลาย X 100
การละลายได้ (Solubility)
ความสามารถในการละลายของสารชนิดหนึ่งในสารอีกชนิดหนึ่งนั้นสามารถหาได้จาก อัตราส่วนระหว่างตัวถูกละลาย กับตัวทำละลาย หรือ อัตราส่วนระหว่างตัวถูกละลาย กับสารละลาย ในสภาวะที่สารละลายนั้นเป็นสารละลายอิ่มตัว ซึ่งสามาถรบอกเป็นความหนาแน่นสูงสุดของสารละลายนั้นได้อีกด้วยซึ่งขึ้นอยู่ กับปัจจัยหลายประการ เช่น แรงระหว่างโมเลกุลของตัวทำละลายกับตัวถูกละลาย อุณหภูมิ ความดัน และปัจจัยอื่นๆ
สมบัติบางประการของสารละลาย
ตัวทำละลายที่เป็นสารบริสุทธิ์เมื่อเติม ตัวถูกละลายลงไปกลายเป็นสารละลายจะทำให้สมบัติของตัวทำละลายเปลี่ยนไป เช่น ความดันไอ จุดเดือด จุดหลอมเหลว สมบัติดังกล่าวของสารละลาย เรียกว่า สมบัติคอลลิเกทีฟ (colligative properties) ซึ่งได้แก่
1. การเพิ่มขึ้นของจุดเดือด (boiling point elevation)
2. การลดลงของจุดเยือกแข็ง (freezing point depression)
3. การลดลงของความดันไอ (vapor pressure lowering)
4. การเกิดแรงดันออสโมซิส (osmosis pressure)



